消化器内視鏡処置時の鎮静

国内臨床試験成績
消化器内視鏡処置を受ける日本人患者を対象とした非盲検非対照試験(REM-IICT-JP02試験:国内第Ⅲ相医師主導臨床試験)1)
1)社内資料:国内第Ⅲ相医師主導臨床試験(REM-IICT-JP02試験、承認時評価資料)
目的
オピオイド鎮痛薬*1併用下で消化器内視鏡処置を受ける日本人患者を対象に、アネレム®の有効性及び安全性を評価する。
試験デザイン
多施設共同、非盲検、非対照試験
対象
オピオイド鎮痛薬併用下で、上部消化管(経口)、大腸、肝胆膵、小腸の内視鏡処置を受ける成人
患者62例(上部消化管25例、大腸27例、肝胆膵7例、小腸3例)
有効性解析対象集団( Full Analysis Set:FAS):62例
安全性解析対象集団(Safety Population:SP):62例
方法
消化器内視鏡処置を受ける患者にオピオイド鎮痛薬を投与し、その直後に初回投与としてアネレム®3mgを15秒以上の時間をかけて緩徐に単回静脈内投与した*2。
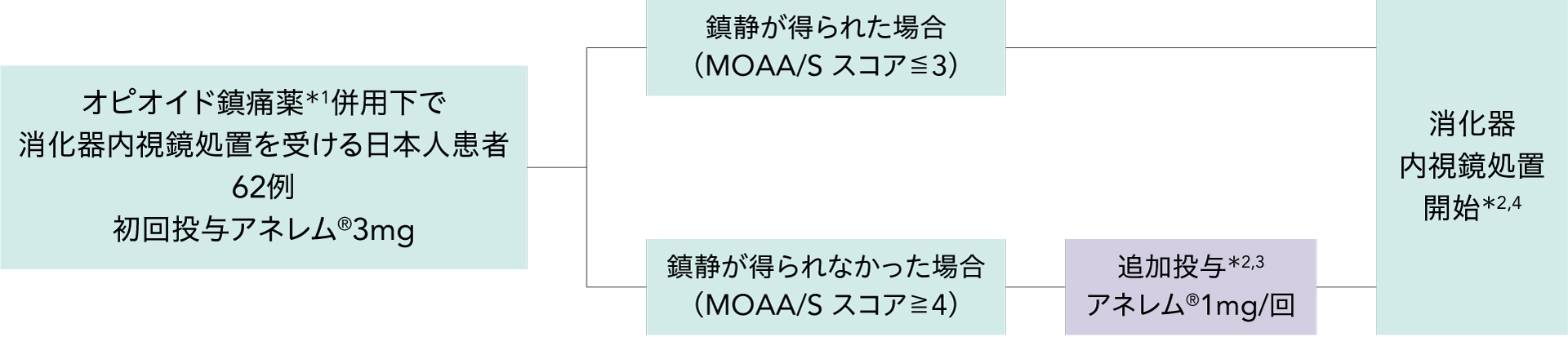
主な選択基準
20歳≦、BMI<30kg/m2、予定する内視鏡処置時間(スコープ挿入から最終抜去まで)が15分を超えると治験責任/分担医師によって判断される者、少なくとも内視鏡処置前日から内視鏡処置翌日までの3日間入院可能な者
*1:ペチジン塩酸塩又はペンタゾシン
*2:75歳以上の高齢者又は45kg未満の低体重者はアネレム®の投与量を半量に減量可とした。
*3:追加投与の上限は5回までとした。
*4:内視鏡処置開始後に覚醒徴候(MOAA/Sスコア5や体動等)が認められ、治験責任/分担医師が追加投与を必要と判断した場合は、アネレム®の追加投与を可とした。

評価項目
〈主要評価項目〉
消化器内視鏡処置における鎮静の成功*5 割合(検証的な解析項目)
内視鏡処置部位別、アネレム®の減量有無別及び必須併用鎮痛薬別の鎮静の成功*5 割合
*5:消化器内視鏡処置における鎮静の成功の定義
以下のすべてを満たす場合に成功とする。
●内視鏡処置開始前に鎮静(MOAA/Sスコア3以下)が得られる
●消化器内視鏡処置の完遂
●内視鏡処置開始後の追加投与の回数が15分間当たり5回を超えない
〈副次評価項目〉
内視鏡処置開始前に鎮静が得られた患者の割合、アネレム®の初回投与から鎮静が得られるまでの時間、鎮静が得られるまでのアネレム®の投与量(内視鏡処置開始までの総投与量)及び投与回数、内視鏡処置中の記憶の有無(Brice質問票を用いて、治験責任/分担医師が評価)、アネレム®最終投与後から退室可能と判断されるまでの時間、内視鏡処置終了から退室可能と判断されるまでの時間 等
〈安全性評価項目〉
有害事象、副作用、臨床検査(血液学的検査、血液生化学検査及び尿検査)、バイタルサイン(血圧、心拍数、呼吸数、SpO2)、心電図検査(12誘導心電図、モニター心電図)、投与部位血管痛の有無、覚醒の評価(覚醒後の再鎮静の有無)、意識消失、用手換気、緊急的なフルマゼニルの投与、内視鏡医以外の医師による緊急対応の有無
解析計画
主要評価項目である消化器内視鏡処置における成功割合及びその正確な両側95%信頼区間を算出した。また、閾値成功割合(p0)を80%*6 としたときの二項検定を行い、p値を算出した。さらに、内視鏡処置部位別、アネレム®の減量有無別及び必須併用鎮痛薬別の成功割合についても同様の解析を行った。
副次評価項目について、基本統計量、患者割合や両側95%CI等を算出した。鎮静が得られるまでのアネレム®の投与量(内視鏡処置開始までの総投与量)は、適切な鎮静(MOAA/Sスコア3以下)が得られた患者を対象に基本統計量を算出した。
アネレム®の初回投与から鎮静が得られるまでの時間、アネレム®最終投与後から退室可能と判断されるまでの時間、内視鏡処置終了から退室可能と判断されるまでの時間は、Kaplan-Meier曲線を作成した。
安全性評価項目は安全性解析対象集団で解析を行った。
*6: 海外第Ⅲ相臨床試験(CNS7056-006試験)2)において、オピオイド鎮痛薬(フェンタニル)併用下でのアネレム®の鎮静の成功割合は91.3%(272/298例)であった。この試験成績等を踏まえ、本試験におけるアネレム®の期待成功割合を95%、閾値成功割合を80%とした。
患者背景[FAS]
有効性解析対象集団における患者背景は以下のとおりでした。
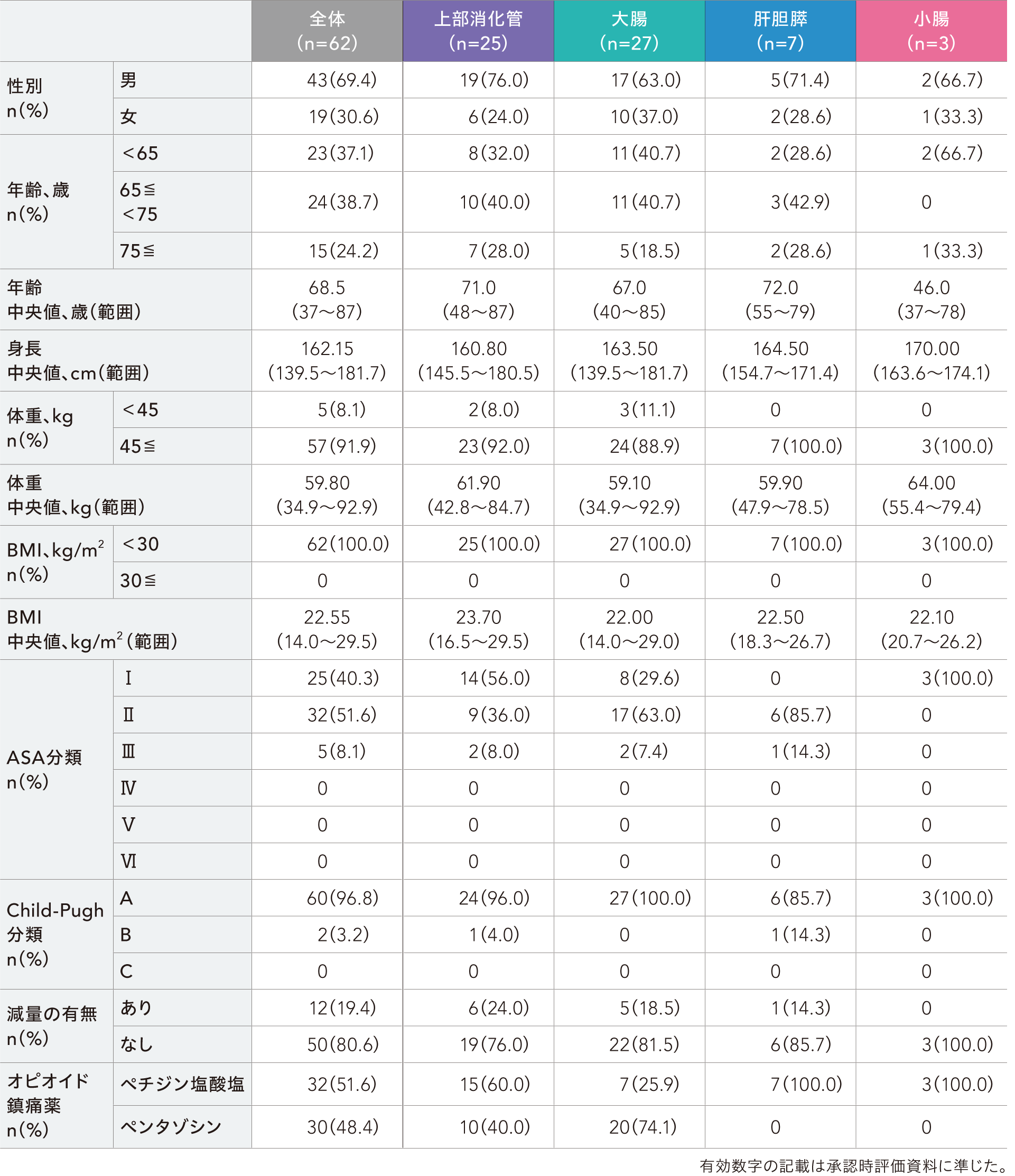
有効性
消化器内視鏡処置における鎮静の成功割合[主要評価項目、FAS]
消化器内視鏡処置における鎮静の成功割合(検証的な解析項目)は、全体で93.5%[95%CI:84.3, 98.2]でした。閾値成功割合(p0)を80%としたときの二項検定の結果はp=0.004であり、閾値成功割合を有意に上回ることが検証されました。
内視鏡処置部位別の鎮静の成功割合は、上部消化管が88.0%[68.8, 97.5]、大腸が100.0%[87.2, 100.0]等でした。
消化器内視鏡処置における鎮静の成功割合
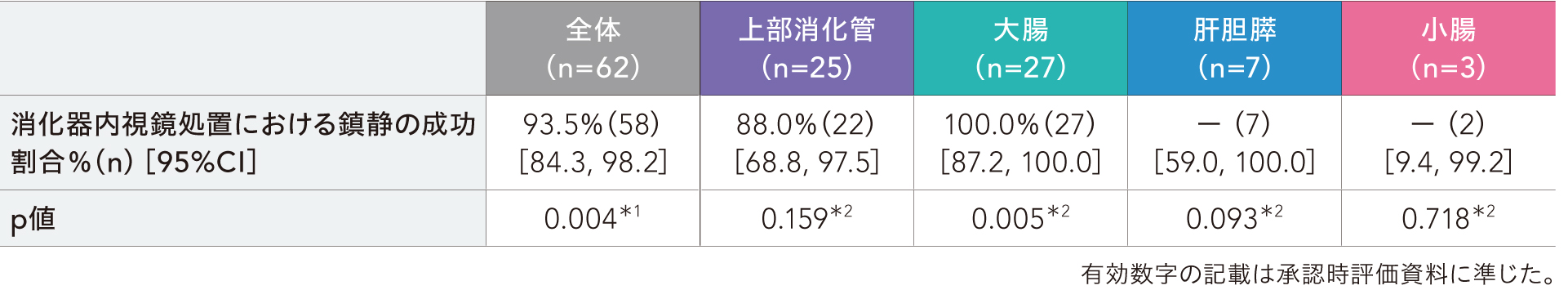
*1:検証的な解析結果、閾値成功割合80%との比較、二項検定
*2:名目上のp値、閾値成功割合80%との比較、二項検定
消化器内視鏡処置におけるアネレム®の減量有無別、
必須併用鎮痛薬別の鎮静の成功割合[主要評価項目、FAS]
75歳以上の高齢者又は45kg未満の低体重者に該当し、アネレム®を減量した患者(12/62例)における鎮静の成功割合は100.0%[95%CI:73.5, 100.0]、減量しなかった患者(50/62例)における鎮静の成功割合は92.0%[80.8, 97.8]でした。
必須併用鎮痛薬別の鎮静の成功割合は、ペチジン塩酸塩が87.5%[71.0, 96.5]、ペンタゾシンが100.0%[88.4, 100.0]でした。
消化器内視鏡処置における鎮静の成功割合
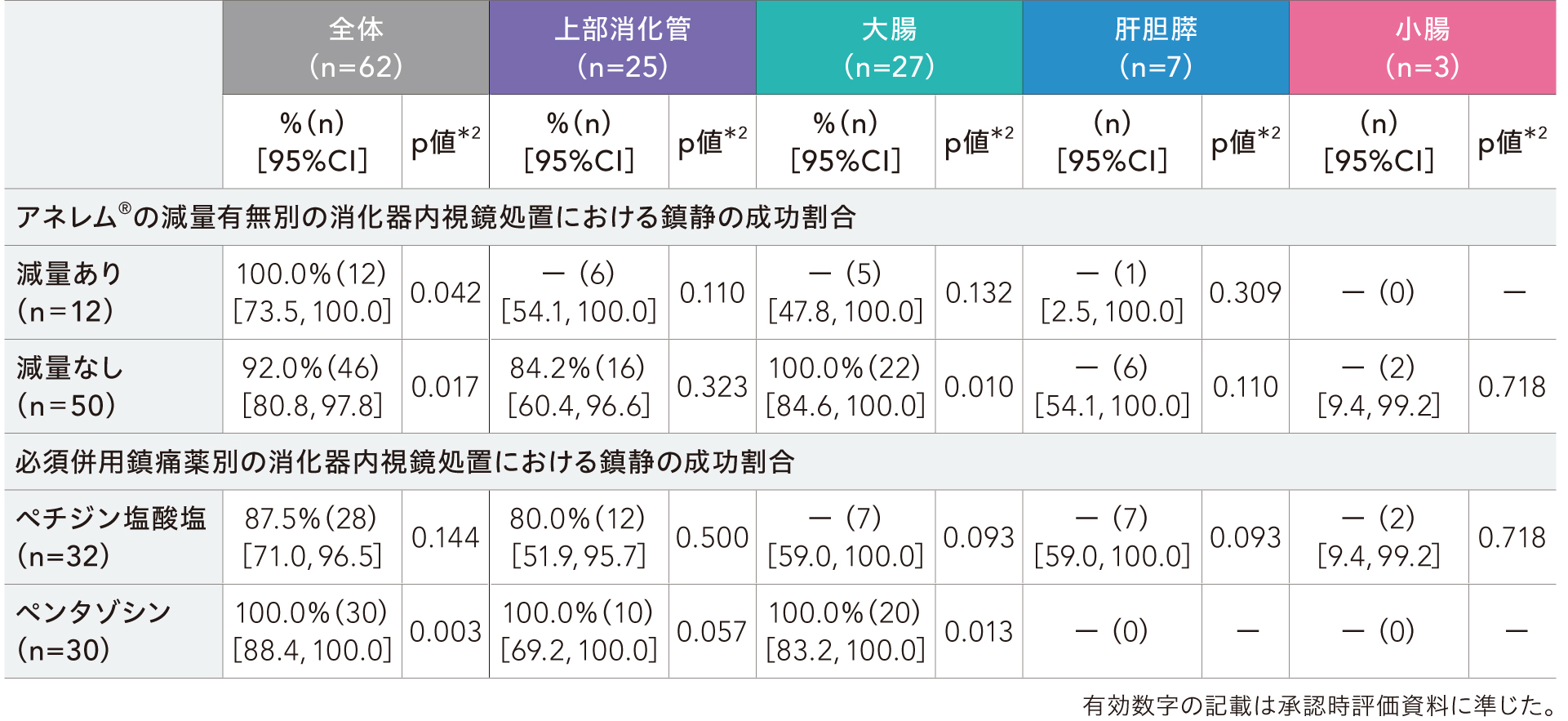
*2:名目上のp値、閾値成功割合80%との比較、二項検定
医療用医薬品製品情報概要等に関する作成要領に基づき、症例数が10例未満における割合の表記は省略しています。
副次評価項目[FAS]
内視鏡処置開始前に鎮静が得られた患者の割合、アネレム®の初回投与から鎮静が得られるまでの時間、鎮静が得られるまでのアネレム®の投与量(内視鏡処置開始までの総投与量)及び投与回数、内視鏡処置中の記憶の有無、アネレム®最終投与後から退室可能と判断されるまでの時間、内視鏡処置終了から退室可能と判断されるまでの時間について評価した結果は以下の表のとおりでした。
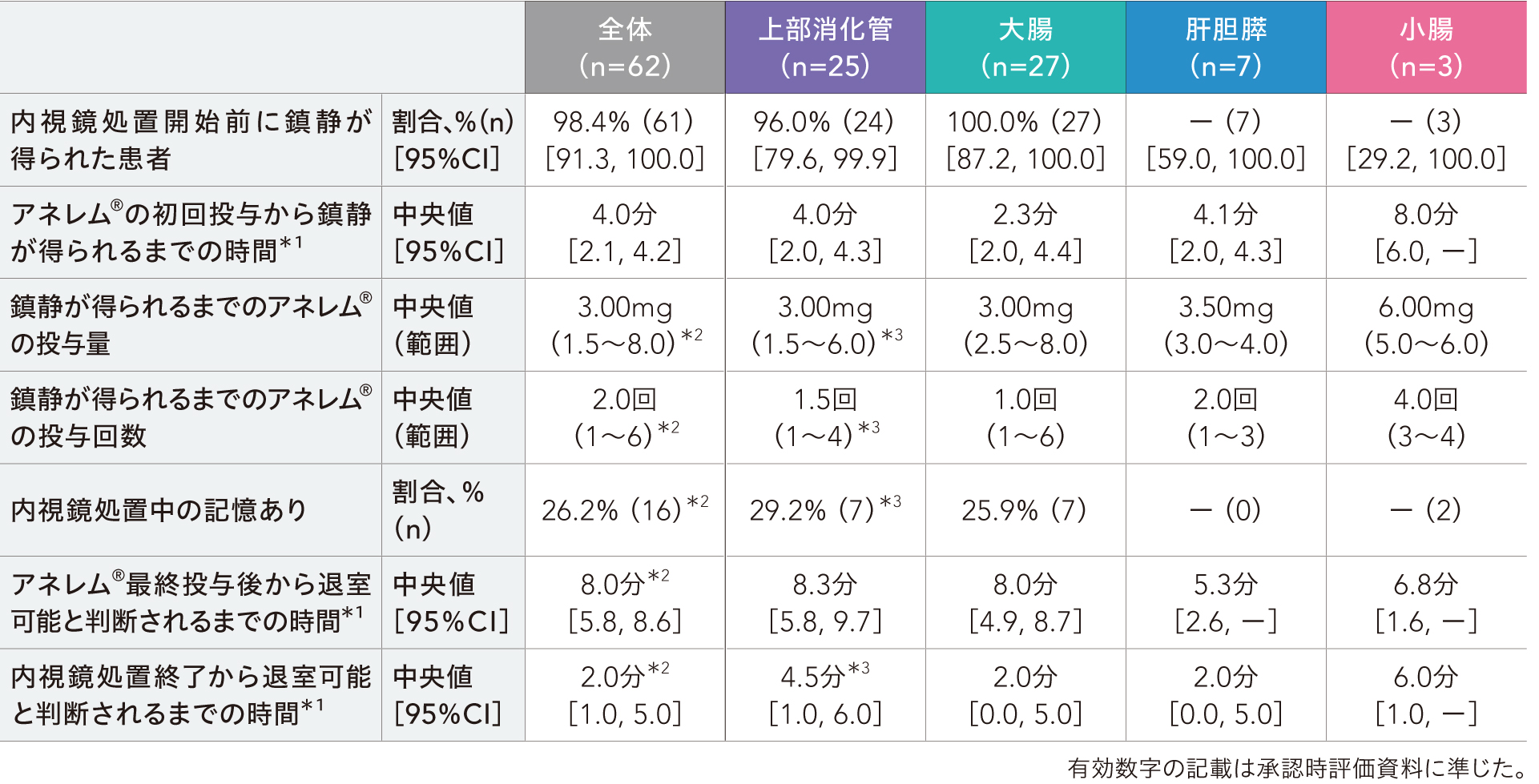
*1:Kaplan-Meier法を用いて算出した。
*2:n=61
*3:n=24
医療用医薬品製品情報概要等に関する作成要領に基づき、症例数が10例未満における割合の表記は省略しています。
補足情報
■内視鏡処置時の時間【FAS】

*1 : n=61 *2 n=24
■アネレム®投与状況【FAS】
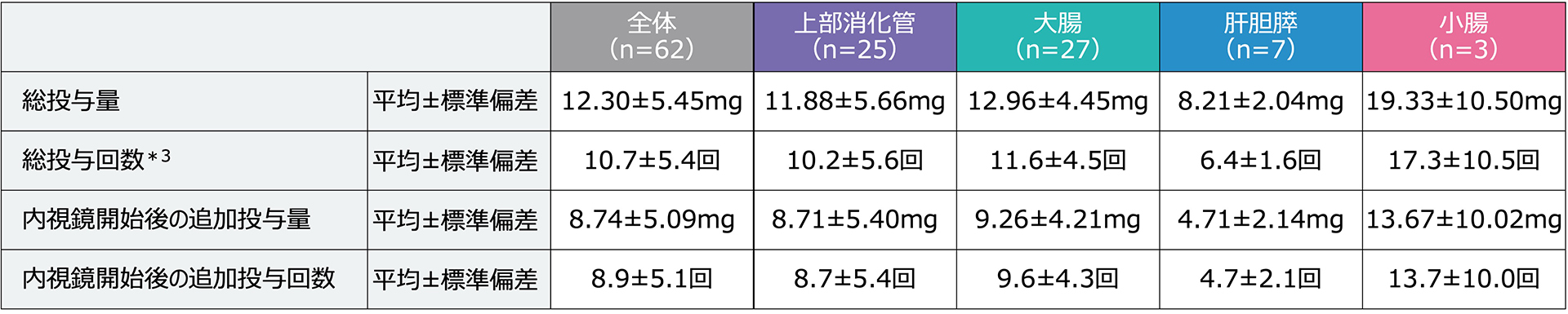
*3 : 総投与回数=1(初回投与回数)+追加投与数
安全性
副作用[安全性評価項目、SP]
安全性解析対象集団62例のうち、副作用発現率は24.2%(15/62例)であり、主な副作用は低酸素症12.9%(8/62例)、悪心4.8%(3/62例)、頭痛3.2%(2/62例)等でした。
本試験において、重篤な有害事象、試験中止に至った有害事象、死亡は認めらせんでした。
■ 主な副作用
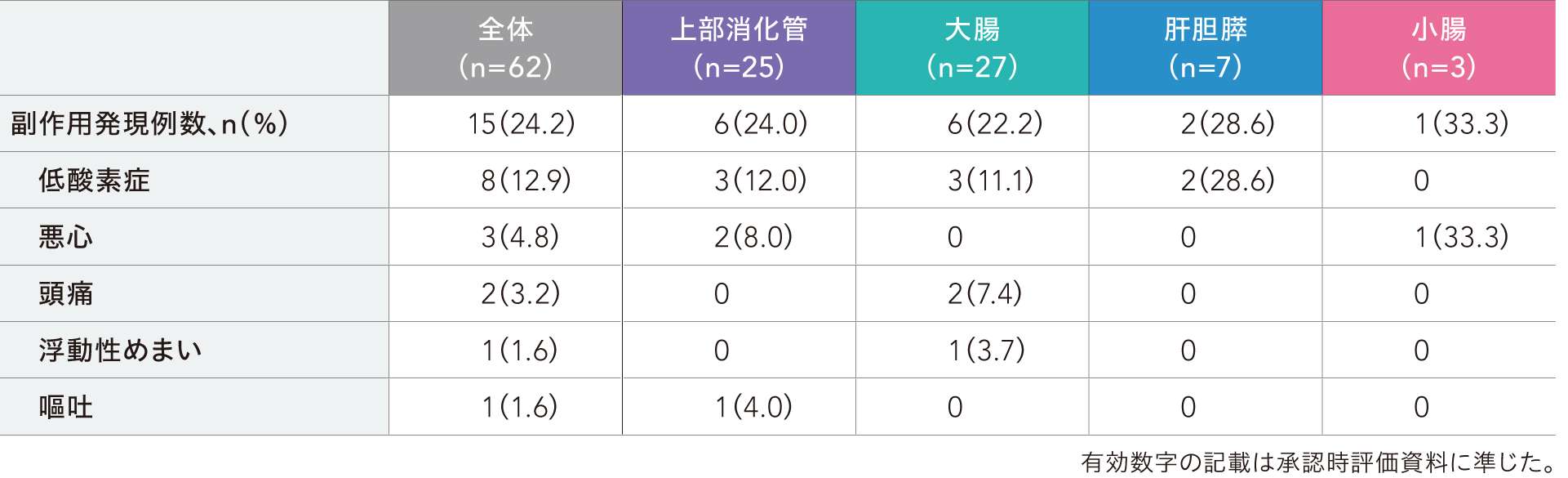
集計に用いた用語はMedDRA v25.0に準じた。
臨床検査値、バイタルサイン、心電図検査の評価
試験期間を通して、臨床検査に関わる有害事象は認められなませんでした。高血圧が1例に認められましたが、非重篤かつ軽度の有害事象であり、アネレム®との関連性はなしと判定されました。心拍数、呼吸数及びSpO2に臨床的に意義のある変動は認められませんでした。低酸素症は8例に認められ、いずれもアネレム®投与中に発現しており、副作用と判定されました。ベースライン時から内視鏡処置終了24時間後までの心電図に臨床的に意義のある変動は認められませんでした。
その他の安全性評価項目
試験期間を通して、投与部位血管痛は認められませんでした。
覚醒後の再鎮静は認められませんでした。意識消失(連続する2評価時点以上でMOAA/Sスコア1以下)は、上部消化管内視鏡処置を受けた1例に認められましたが、一時的な事象であり、有害事象とは判断されませんでした。用手換気が実施された患者はいませんでした。
また、緊急的にフルマゼニルを投与された患者はおらず、内視鏡医以外の医師による緊急対応を受けた患者も認められませんでした。
2)社内資料:海外第Ⅲ相臨床試験(CNS7056-006試験、承認時参考資料)











